Carbon dioxide hay cacbonic Oxide (tên gọi khác: thán khí, anhydride carbonic, khí carbonic) là một hợp chất ở điều kiện bình thường có dạng khí trong khí quyển Trái Đất, bao gồm một nguyên tử carbon và hai nguyên tử oxy. Là một hợp chất hóa học được biết đến rộng rãi, nó thường xuyên được gọi theo công thức hóa học là CO2. Trong dạng rắn, nó được gọi là băng khô hoặc đá khô.
Carbon dioxide thu được từ nhiều nguồn khác nhau, gồm có cả khí thoát ra từ những núi lửa, loại sản phẩm cháy của những hợp chất hữu cơ và hoạt động giải trí hô hấp của những sinh vật sống hiếu khí. Nó cũng được một số ít vi sinh vật sản xuất từ sự lên men và sự hô hấp của tế bào. Các loài thực vật hấp thụ carbon dioxide trong quy trình quang hợp, và sử dụng cả carbon và oxy để tạo ra những cacbohydrat. Ngoài ra, thực vật cũng giải phóng oxy trở lại khí quyển, oxy này sẽ được những sinh vật dị dưỡng sử dụng trong quy trình hô hấp, tạo thành một quy trình. Nó xuất hiện trong khí quyển Trái Đất với nồng độ thấp và tác động ảnh hưởng như một khí gây hiệu ứng nhà kính. Nó là thành phần chính trong quy trình carbon .
Mục lục nội dung
Các thuộc tính hóa-lý[sửa|sửa mã nguồn]
Carbon dioxide là một khí không màu mà khi hít thở phải ở nồng độ cao ( nguy khốn do nó gắn liền với rủi ro đáng tiếc ngạt thở ) tạo ra vị chua trong miệng và cảm xúc nhói ở mũi và cổ họng. Các hiệu ứng này là do khí hòa tan trong màng nhầy và nước bọt, tạo ra dung dịch yếu của axit cacbonic .
Tỷ trọng riêng của nó ở 25 °C là 1,98 kg·m−3, nặng hơn khoảng 1,5 lần không khí. Phân tử carbon dioxide (O = C = O) chứa hai liên kết đôi và có hình dạng tuyến tính. Nó không có lưỡng cực điện. Do nó là hợp chất đã bị oxy hóa hoàn toàn nên về mặt hóa học nó không hoạt động lắm và cụ thể là không cháy.
Bạn đang đọc: Carbon dioxide – Wikipedia tiếng Việt
Ở nhiệt độ dưới – 78 °C, carbon dioxide ngưng tụ lại thành những tinh thể màu trắng gọi là băng khô. Carbon dioxide lỏng chỉ được tạo ra dưới áp suất trên 5,1 bar ; ở điều kiện kèm theo áp suất khí quyển, nó chuyển trực tiếp từ những pha khí sang rắn hay ngược lại theo một quy trình gọi là thăng hoa .Nước sẽ hấp thụ một lượng nhất định carbon dioxide, và nhiều hơn lượng này khi khí bị nén. Khoảng 1 % carbon dioxide hòa tan chuyển hóa thành axit cacbonic. Axit cacbonic phân ly một phần thành những ion bicacbonat ( HCO3 − ) và cacbonat ( CO32 − ) .Khi một nguồn lửa được đưa vào ống thử có chứa carbon dioxide thì ngọn lửa sẽ tắt ngay lập tức do carbon dioxide thường thì không duy trì sự cháy, tuy nhiên nếu là sự cháy của những sắt kẽm kim loại mang tính khử cao như Mg, Zn thì carbon bị khử, tạo ra Oxide sắt kẽm kim loại và muội than. ( Một số loại bình cứu hỏa chứa carbon dioxide hay những chất khi phản ứng với nhau sẽ tạo ra nó dùng để dập lửa ). Để xác nhận tiếp theo là khí này là carbon dioxide thì khí được dẫn qua dung dịch calci hydroxide ( Ca ( OH ) 2 ) trong. Dung dịch calci hydroxide sẽ chuyển thành kết tủa màu trắng do sự tạo thành calci carbonat ( CaCO3 ) .
Carbon dioxide lỏng và rắn là chất làm lạnh quan trọng, đặc biệt quan trọng là trong công nghiệp thực phẩm, trong đó chúng tham gia vào quy trình tàng trữ và luân chuyển những loại kem lạnh và những thực phẩm ướp lạnh .Carbon dioxide được sử dụng để sản xuất nước giải khát cacbonat hóa và nước soda. Theo truyền thống cuội nguồn, quy trình cacbonat hóa trong bia và vang nổ có được do lên men tự nhiên, nhưng 1 số ít nhà phân phối cacbonat hóa những đồ uống này một cách tự tạo .Bột nở sử dụng trong những loại bánh nướng tạo ra khí cacbonic làm cho khối bột bị phình to ra, do tạo ra những lỗ xốp chứa bọt khí. Men bánh mì tạo ra khí cacbonic bằng sự lên men trong khối bột, trong khi những loại bột nở hóa học giải phóng ra khí cacbonic khi bị nung nóng hoặc bị công dụng với những axit .Carbon dioxide thường thì cũng được sử dụng như là khí điều áp rẻ tiền, không cháy. Các áo phao cứu trợ cứu hộ cứu nạn thường thì chứa những hộp nhỏ chứa carbon dioxide đã nén để nhanh gọn thổi phồng lên. Các ống thép chứa cacbonic nén cũng được bán để cup cấp khí nén cho súng hơi, bi sơn, bơm lốp xe đạp điện, cũng như để làm nước khoáng xenxe. Sự bốc hơi nhanh gọn của carbon dioxide lỏng được sử dụng để gây nổ trong những mỏ than .Carbon dioxide dập tắt lửa, và 1 số ít bình cứu hỏa, đặc biệt quan trọng là những loại được thiết kể để dập cháy do điện, có chứa carbon dioxide lỏng bị nén. carbon dioxide cũng được sử dụng như thể thiên nhiên và môi trường khí cho công nghệ tiên tiến hàn, mặc dầu trong hồ quang thì nó phản ứng với phần nhiều những sắt kẽm kim loại. Nó được sử dụng thoáng rộng trong công nghiệp xe hơi mặc dầu có chứng cứ đáng kể cho thấy khi hàn trong môi trường tự nhiên này thì mối hàn giòn hơn so với những mối hàn trong thiên nhiên và môi trường những khí trơ, và những mối hàn này theo thời hạn sẽ giảm phẩm cấp do sự tạo thành của axít cacbonic. Nó được sử dụng thao tác này đa phần là do nó rẻ tiền hơn nhiều so với những khí trơ như agon hay heli .Carbon dioxide lỏng là một dung môi tốt cho nhiều hợp chất hữu cơ, và được dùng để vô hiệu cafein từ cafe. Nó cũng mở màn nhận được sự chú ý quan tâm của công nghiệp dược phẩm và 1 số ít ngành công nghiệp chế biến hóa chất khác do nó là chất sửa chữa thay thế ít độc hơn cho những dung môi truyền thống lịch sử như những chloride hữu cơ ( xem hóa học xanh ) .
Thực vật cần có carbon dioxide để thực hiện việc quang hợp, và các nhà kính có thể được làm giàu bầu khí quyển của chúng bằng việc bổ sung CO2 nhằm kích thích sự tăng trưởng của thực vật. Người ta cũng đề xuất ý tưởng cho carbon dioxide từ các nhà máy nhiệt điện đi qua các ao để phát triển tảo và sau đó chuyển hóa chúng thành nguồn nhiên liệu điezen sinh học. Nồng độ cao của carbon dioxide trong khí quyển tiêu diệt có hiệu quả nhiều loại sâu hại. Các nhà kính được nâng nồng độ CO2 tới 10.000 ppm (1%) trong vài giờ để tiêu diệt các loại sâu bệnh như rầy trắng (họ Aleyrodidae), nhện v.v.
Trong y học, tới 5 % carbon dioxide được thêm vào oxy nguyên chất để trợ thở sau khi ngừng thở và để không thay đổi cân đối O2 / CO2 trong máu .Một dạng phổ cập của laze khí công nghiệp là laze carbon dioxide, sử dụng carbon dioxide làm môi trường tự nhiên .Carbon dioxide cũng hay được bơm vào hay gần với những giếng dầu. Nó có công dụng như là tác nhân nén và khi hòa tan trong dầu thô dưới lòng đất thì nó làm giảm đáng kể độ nhớt của dầu thô, tạo điều kiện kèm theo để dầu chảy nhanh hơn trong lòng đất vào những giếng hút. Trong những mỏ dầu đã hoàn thành xong thì một mạng lưới hệ thống ống đồ sộ được sử dụng để chuyển carbon dioxide tới những điểm bơm .
Băng khô là thương hiệu cho carbon dioxide rắn (đóng băng). Thuật ngữ này được Prest Air Devices tạo ra năm 1925 (công ty thành lập năm 1923 tại thành phố Long Island, New York).
Băng khô, dưới áp suất thường, không nóng chảy thành carbon dioxide lỏng mà thăng hoa trực tiếp thành dạng khí ở – 78,5 °C ( – 109,3 °F ). Vì thế nó được gọi là ” băng khô ” như là cách gọi để so sánh với băng ” ướt ” ( nước đá thường thì ) .Băng khô được sản xuất bằng cách nén khí carbon dioxide thành dạng lỏng, vô hiệu nhiệt gây ra bởi quy trình nén ( xem định luật Charles ), và sau đó cho carbon dioxide lỏng co và giãn nhanh. Sự co và giãn này làm giảm nhiệt độ và làm cho một phần CO2 bị ngừng hoạt động thành ” tuyết “, sau đó ” tuyết ” này được nén thành những viên hay khối .
 Hoa KỳBăng khô được sử dụng để làm lạnh đồ uống tại Công viên TT, thành phố Thành Phố New York
Hoa KỳBăng khô được sử dụng để làm lạnh đồ uống tại Công viên TT, thành phố Thành Phố New York
- Làm lạnh thực phẩm, các mẫu sinh học và các mặt hàng mau hỏng khác.
- Sản xuất “sương mù băng khô” để tạo các hiệu ứng đặc biệt. Khi băng khô tiếp xúc với nước thì carbon dioxide đóng băng thăng hoa thành hỗn hợp khí carbon dioxide lạnh và không khí lạnh ẩm ướt. Điều này sinh ra sự ngưng tụ và hình thành sương mù; xem thêm máy tạo sương mù. Hiệu ứng sương mù của hỗn hợp băng khô với nước được tạo ra tốt nhất là với nước ấm.
- Các viên nhỏ băng khô (thay vì cát) được bắn vào bề mặt cần làm sạch. Băng khô không cứng như cát, nhưng nó tăng tốc quá trình bằng sự thăng hoa để “không còn gì” tồn tại trên bề mặt cần làm sạch và gần như không tạo ra nhiều bụi gây hại phổi.
- Tăng gây mưa từ các đám mây hay làm giảm độ dày của mây nhờ sự kết tinh nước trong mây.
- Sản xuất khí carbon dioxide do cần thiết trong các hệ thống như thùng nhiên liệu hệ thống trơ trong các máy bay B-47.
- Các ống lót trục bằng đồng thau hay kim loại khác được cho vào băng khô để làm chúng co lại sao cho chúng sẽ khớp với kích thước trong của lỗ trục. Khi các ống lót này ấm trở lại, chúng nở ra và trở nên cực kỳ khít nhau.
Do những đặc trưng đơn cử của mình, băng khô yên cầu phải có sự phòng ngừa đặc biệt quan trọng khi tiếp xúc. Nó cực lạnh thế cho nên không nên cho tiếp xúc trực tiếp với da ( nghĩa là cần đeo găng cách nhiệt thích hợp ). Nó tiếp tục thăng hoa thành khí cacbonic, cho nên vì thế nó không hề tàng trữ trong những thùng chứa có nắp đậy do áp suất tạo ra sẽ nhanh gọn phá vỡ thùng do bị nổ. Khí thăng hoa cần thông gió tốt ; nếu không nó hoàn toàn có thể tràn ngập khoảng trống quanh đó và làm cho người ta không thở được. Sự chăm sóc đặc biệt quan trọng so với những thiết bị thông gió là thiết yếu. Những người tiếp xúc với băng khô cần phải được cảnh báo nhắc nhở là carbon dioxide nặng hơn không khí và sẽ chìm xuống dưới sàn. Một số thị trường yên cầu những người mua băng khô phải từ 18 tuổi trở lên .
Carbon dioxide là loại sản phẩm ở đầu cuối trong khung hình sinh vật có sự tích lũy nguồn năng lượng từ việc phân hủy đường hay chất béo với oxy như là một phần của sự trao đổi chất của chúng, trong một quy trình được biết đến như thể sự hô hấp của tế bào. Nó gồm có tổng thể những loài thực vật, động vật hoang dã, nhiều loại nấm và 1 số ít vi trùng. Trong những động vật hoang dã bậc cao, carbon dioxide vận động và di chuyển trong máu từ những mô của khung hình tới phổi và ở đây nó bị thải ra ngoài .Hàm lượng carbon dioxide trong không khí trong lành là khoảng chừng 0,04 %, và trong không khí bị thải ra từ sự thở là khoảng chừng 4,5 %. Khi thở trong không khí với nồng độ cao ( khoảng chừng 5 % theo thể tích ), nó là ô nhiễm so với con người và những động vật hoang dã khác .Hemoglobin, phân tử chuyên chở oxy chính trong hồng cầu, hoàn toàn có thể chở cả oxy và carbon dioxide, mặc dầu theo những phương pháp trọn vẹn khác nhau. Sự suy giảm link với oxy trong máu do sự tăng mức carbon dioxide được biết đến như là hiệu ứng Haldane, và nó là quan trọng trong việc luân chuyển carbon dioxide từ những mô tới phổi. trái lại, sự tăng áp suất thành phần của CO2 hay pH thấp hơn sẽ sinh ra sự rút bớt oxy từ hemoglobin. Hiệu ứng này gọi là hiệu ứng Bohr .
Theo nghiên cứu của USDA [1][liên kết hỏng], sự thở của một người trung bình mỗi ngày sinh ra khoảng 450 lít (khoảng 900 gam) carbon dioxide.
CO2 được luân chuyển trong máu theo ba cách khác nhau. Phần lớn trong chúng ( khoảng chừng 80 % – 90 % ) được những enzym cacbonic anhydraz chuyển hóa thành những ion bicacbonat HCO3 − trong những tế bào hồng cầu. 5 % – 10 % được hòa tan trong huyết tương và 5 % – 10 % link với hemoglobin thành những hợp chất cacbamin. Phần trăm đúng mực nhờ vào vào đó là máu ở động mạch hay tĩnh mạch .Hemoglobin link với CO2 không giống như link với oxy ; CO2 link với những nhóm chứa N trên 4 chuỗi globin. Tuy nhiên, do những hiệu ứng khác khu vực hoạt hóa trên phân tử hemoglobin, link của CO2 làm giảm lượng oxy được link so với áp suất thành phần nhất định của oxy .Carbon dioxide hoàn toàn có thể là một trong những chất trung gian để tự kiểm soát và điều chỉnh việc phân phối máu theo khu vực. Nếu nồng độ của nó cao thì những mao mạch nở ra để cho nhiều máu hơn đến những mô .Các ion bicacbonat là đa phần trong việc kiểm soát và điều chỉnh pH của máu. Do tần suất thở có tác động ảnh hưởng tới mức CO2 trong máu, nên nhịp thở quá chậm hay quá nông sẽ sinh ra hiện tượng kỳ lạ nhiễm axít hô hấp, trong khi nhịp thở quá nhanh sinh ra trong những chứng thở quá nhanh sẽ dẫn đến nhiễm kiềm hô hấp .
Một điều thú vị là mặc dù oxy là chất cần thiết của quá trình trao đổi chất của cơ thể, nhưng không phải nồng độ thấp của oxy kích thích sự hô hấp mà lại là nồng độ cao của carbon dioxide. Kết quả là, sự hô hấp trong không khí loãng (áp suất thấp) hay hỗn hợp khí không có oxy (ví dụ nitơ nguyên chất) dẫn đến sự bất tỉnh mà không cần có các vấn đề về hệ hô hấp của cá thể đó. Nó là đặc biệt nguy hiểm cho các phi công lái máy bay chiến đấu bay ở cao độ lớn, và nó cũng là lý do giải thích tại sao các hướng dẫn tại các máy bay thương mại trong trường hợp sụt áp suất trong khoang thì người ta cần phải sử dụng mặt nạ thở oxy cho chính mình trước khi giúp người khác—nếu không thì chính người đó sẽ chịu rủi ro bất tỉnh mà không hề được cảnh báo trước về nguy hiểm sắp xảy ra.
Thực vật hấp thụ carbon dioxide từ khí quyển trong quy trình quang hợp. Carbon dioxide được thực vật ( với nguồn năng lượng từ ánh sáng Mặt Trời ) sử dụng để sản xuất ra những chất hữu cơ bằng tổng hợp nó với nước. Các phản ứng này giải phóng ra oxy tự do. Đôi khi carbon dioxide được bơm thêm vào những nhà kính để thôi thúc thực vật tăng trưởng. Thực vật cũng giải phóng ra CO2 trong quy trình hô hấp của nó, nhưng toàn diện và tổng thể thì chúng làm giảm lượng CO2 .Các số lượng giới hạn của OSHA cho nồng độ carbon dioxide tại nơi thao tác là 0,5 % cho thời hạn dài, tối đa tới 3 % cho phơi nhiễm ngắn ( tối đa 10 phút ). OSHA cho rằng những nồng độ trên 4 % là ” nguy khốn ngay lập tức so với sức khỏe thể chất và sự sống “. Những người thở không khí chứa trên 5 % carbon dioxide trên 30 phút có những triệu chứng tăng anhydride cacbonic máu cấp tính, trong khi việc thở với nồng độ carbon dioxide từ 7 % – 10 % hoàn toàn có thể làm bất tỉnh nhân sự trong vài phút. Carbon dioxide, dù là dạng khí hay dạng rắn, chỉ được tiếp xúc trong những môi trường tự nhiên / khu vực thông gió tốt .
Xem thêm: Khí trong máu động mạch.
Khí quyển Trái Đất[sửa|sửa mã nguồn]
 2 trong khí quyển, đo tại Nồng độ COtrong khí quyển, đo tại Mauna LoaVào thời gian năm 2004, khí quyển Trái Đất chứa khoảng chừng 0,038 % theo thể tích ( 380 µL / L hay ppm ) hoặc 0,053 % theo khối lượng là CO2. Nó tương tự với 2,7 × 1012 tấn CO2. Do có nhiều đất đai hơn ( và do đó nhiều thực vật hơn ) nên ở bắc bán cầu khi so với nam bán cầu có sự giao động hàng năm vào khoảng chừng 5 µL / L, sự giao động này lên tới đỉnh vào tháng 5 và xuống tối thiểu vào tháng 10 khi kết thúc mùa sinh trưởng ở bắc bán cầu, khi mà khối lượng những chất sinh học trên hành tinh là lớn nhất .Mặc dù nồng độ thấp nhưng CO2 là một thành phần cực kỳ quan trọng trong khí quyển Trái Đất, do nó hấp thụ bức xạ hồng ngoại và làm tăng hiệu ứng nhà kính .Carbon dioxide nguyên thủy trong khí quyển của Trái Đất được tạo ra trong hoạt động giải trí của những núi lửa ; nó là cốt yếu để làm ấm và không thay đổi khí hậu dẫn đến sự sống. Hoạt động núi lửa ngày này giải phóng khoảng chừng 130 – 230 triệu tấn carbon dioxide mỗi năm. Lượng khí này xê dịch 1 % lượng carbon dioxide do những hoạt động giải trí của con người tạo ra .
2 trong khí quyển, đo tại Nồng độ COtrong khí quyển, đo tại Mauna LoaVào thời gian năm 2004, khí quyển Trái Đất chứa khoảng chừng 0,038 % theo thể tích ( 380 µL / L hay ppm ) hoặc 0,053 % theo khối lượng là CO2. Nó tương tự với 2,7 × 1012 tấn CO2. Do có nhiều đất đai hơn ( và do đó nhiều thực vật hơn ) nên ở bắc bán cầu khi so với nam bán cầu có sự giao động hàng năm vào khoảng chừng 5 µL / L, sự giao động này lên tới đỉnh vào tháng 5 và xuống tối thiểu vào tháng 10 khi kết thúc mùa sinh trưởng ở bắc bán cầu, khi mà khối lượng những chất sinh học trên hành tinh là lớn nhất .Mặc dù nồng độ thấp nhưng CO2 là một thành phần cực kỳ quan trọng trong khí quyển Trái Đất, do nó hấp thụ bức xạ hồng ngoại và làm tăng hiệu ứng nhà kính .Carbon dioxide nguyên thủy trong khí quyển của Trái Đất được tạo ra trong hoạt động giải trí của những núi lửa ; nó là cốt yếu để làm ấm và không thay đổi khí hậu dẫn đến sự sống. Hoạt động núi lửa ngày này giải phóng khoảng chừng 130 – 230 triệu tấn carbon dioxide mỗi năm. Lượng khí này xê dịch 1 % lượng carbon dioxide do những hoạt động giải trí của con người tạo ra .
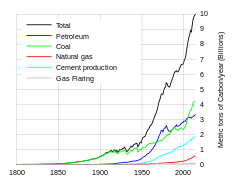 Sự thải khí carbon dioxide toàn thế giới từ năm 1751 đến năm 2004
Sự thải khí carbon dioxide toàn thế giới từ năm 1751 đến năm 2004
Từ đầu thời kỳ cách mạng công nghiệp, nồng độ CO2 trong khí quyển đã tăng khoảng 110 µL/L hay khoảng 40%, phần lớn trong số này được giải phóng từ năm 1945 đến nay. Các đo đạc hàng tháng tại Mauna Loa [2] Lưu trữ 2004-12-10 tại Wayback Machine từ năm 1958 chỉ ra sự tăng từ 316 µL/L trong năm đó tới 376 µL/L năm 2003, tổng thể tăng 60 µL/L trong lịch sử 44 năm đo đạc. Các nhiên liệu hóa thạch như than và dầu mỏ bị đốt là nguyên nhân chính trong sự gia tăng của CO2 do con người tạo ra; Sự tàn phá rừng là nguyên nhân thứ hai. Năm 1997, các đám cháy than bùn ở Indonesia có thể giải phóng tới 13%–40% lượng dioxide carbon do nhiên liệu hóa thạch tạo ra. Nhiều công nghệ khác nhau đã được giới thiệu nhằm làm giảm lượng carbon dioxide dư thừa khỏi khí quyển. Không phải toàn bộ lượng CO2 được giải phóng ra tồn tại trong không khí; một số được các đại dương hoặc sinh quyển hấp thụ. Tỷ lệ CO2 tỏa ra trên sự tăng của CO2 trong khí quyển được biết đến như là tỷ lệ bay lên (Keeling và những người khác, 1995); nó dao động theo các trung bình ngắn hạn nhưng thông thường là 57% cao hơn đối với các chu kỳ dài hơn (5 năm).
 Ô nhiễm khói và ôzôn từ những đám cháy ở Indonesia năm 1997 .Thuyết ” sự ấm toàn thế giới ” ( GWT ) dự báo là sự ngày càng tăng lượng CO2 trong khí quyển có xu thế làm trầm trọng thêm hiệu ứng nhà kính và vì vậy góp thêm phần vào sự ấm toàn thế giới. Hiệu ứng của carbon dioxide tạo ra từ sự cháy so với khí hậu được gọi là hiệu ứng Callendar .
Ô nhiễm khói và ôzôn từ những đám cháy ở Indonesia năm 1997 .Thuyết ” sự ấm toàn thế giới ” ( GWT ) dự báo là sự ngày càng tăng lượng CO2 trong khí quyển có xu thế làm trầm trọng thêm hiệu ứng nhà kính và vì vậy góp thêm phần vào sự ấm toàn thế giới. Hiệu ứng của carbon dioxide tạo ra từ sự cháy so với khí hậu được gọi là hiệu ứng Callendar .
Thay đổi trong quá khứ[sửa|sửa mã nguồn]
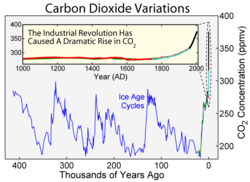 2 trong 400.000 năm gần đâyNồng độ COtrong 400.000 năm gần đâyPhương pháp trực tiếp nhất để đo nồng độ carbon dioxide trong khí quyển cho những thời kỳ trước việc lấy mẫu trực tiếp là đo những bọt khí bị giữ lại trong những chỏm băng ở Nam Cực hay Greenland. Nghiên cứu được đồng ý thoáng đãng nhất là từ những loại lấy từ Nam Cực và chỉ ra rằng mức CO2 trong khí quyển là khoảng chừng 260 – 280 µL / L ngay trước khi khí thải công nghiệp khởi đầu và nó không xê dịch nhiều với mức này trong khoảng chừng 10.000 năm trước đó .Ghi chép về lõi băng dài nhất đến từ Đông Nam Cực, tại đó băng được lấy mẫu đến niên đại khoảng chừng 650.000 năm trước. [ 3 ] Trong thời hạn này, nồng độ carbon dioxide trong khí quyển đã giao động trong khoảng chừng 180 – 210 µL / L trong những thời kỳ băng hà, tăng lên tới 280 – 300 µL / L trong những thời kỳ giữa những kỷ băng hà ấm cúng hơn .
2 trong 400.000 năm gần đâyNồng độ COtrong 400.000 năm gần đâyPhương pháp trực tiếp nhất để đo nồng độ carbon dioxide trong khí quyển cho những thời kỳ trước việc lấy mẫu trực tiếp là đo những bọt khí bị giữ lại trong những chỏm băng ở Nam Cực hay Greenland. Nghiên cứu được đồng ý thoáng đãng nhất là từ những loại lấy từ Nam Cực và chỉ ra rằng mức CO2 trong khí quyển là khoảng chừng 260 – 280 µL / L ngay trước khi khí thải công nghiệp khởi đầu và nó không xê dịch nhiều với mức này trong khoảng chừng 10.000 năm trước đó .Ghi chép về lõi băng dài nhất đến từ Đông Nam Cực, tại đó băng được lấy mẫu đến niên đại khoảng chừng 650.000 năm trước. [ 3 ] Trong thời hạn này, nồng độ carbon dioxide trong khí quyển đã giao động trong khoảng chừng 180 – 210 µL / L trong những thời kỳ băng hà, tăng lên tới 280 – 300 µL / L trong những thời kỳ giữa những kỷ băng hà ấm cúng hơn .
Một số nghiên cứu đã gây tranh luận về sự ổn định của mức CO2 trong thời kỳ giữa các kỷ băng hà gần đây nhất (10.000 năm cuối). Dựa trên phân tích các lá hóa thạch, Wagner và những người khác cho rằng mức CO2 trong thời kỳ 7–10.000 năm trước là cao hơn một cách đáng kể (≈ 300 µL/L) và chứa các thay đổi đáng kể mà có thể có tương quan với các thay đổi khí hậu. Các tuyên bố khác gây tranh cãi là giả thiết cho rằng chúng có lẽ phản ánh các vấn đề định cỡ hơn là các thay đổi thực sự của CO2. Liên quan đến tranh cãi này là các quan sát lõi băng ở Greenland thông thường cho các giá trị của CO2 cao hơn và biến đổi nhiều hơn so với các phép đo tương tự tại Nam Cực. Tuy nhiên, các nhóm chịu trách nhiệm cho các đo đạc này (ví dụ Smith và những người khác tin rằng các thay đổi trong lõi băng Greenland được tạo ra do sự phân hủy tại chỗ (in situ) của bụi calci cacbonat tìm thấy trong băng. Khi mức độ bụi trong các lõi băng Greenland là thấp gần như bằng mức ở lõi băng Nam Cực thì các báo cáo của các nhà nghiên cứu cũng gần như cho một kết quả giữa các phép đo tại hai nơi này.
 Các đổi khác của carbon dioxide từ thời Phanerozoic ( 542 triệu năm trước ). Thời kỳ gần đây nằm bên trái của biểu đồ, và nó có vẻ như là 550 triệu năm trước thì nồng độ carbon dioxide cao hơn đáng kể so với ngày này .
Các đổi khác của carbon dioxide từ thời Phanerozoic ( 542 triệu năm trước ). Thời kỳ gần đây nằm bên trái của biểu đồ, và nó có vẻ như là 550 triệu năm trước thì nồng độ carbon dioxide cao hơn đáng kể so với ngày này .
Trên biểu thời gian dài hơn, các phép đo đại diện khác nhau được sử dụng để cố gắng xác định mức carbon dioxide trong khí quyển hàng triệu năm trước. Các phép đo này bao gồm các tỷ lệ đồng vị bo và carbon trong các dạng trầm tích đại dương nào đó cũng như số lượng khí khổng quan sát được trên các lá hóa thạch. Trong khi các phép đo này ít chính xác hơn về nồng độ carbon dioxide so với việc đo lõi băng thì ở đây có chứng cứ cho thấy các nồng độ CO2 rất cao (> 3.000 µL/L) trong khoảng 600–400 triệu năm trước và trong khoảng 200–150 triệu năm trước.[4] Lưu trữ 2007-04-27 tại Wayback Machine. Trên biểu thời gian dài, hàm lượng CO2 khí quyển được xác định theo cân bằng giữa các quá trình địa hóa học (bao gồm carbon hữu cơ bị chôn vùi trong các trầm tích, đá silicat phong hóa) và tác động của núi lửa. Hiệu ứng ròng của sự không cân bằng nhẹ trong chu trình carbon trên hàng chục đến hàng trăm triệu năm đã làm giảm CO2 khí quyển. Các tốc độ của các quá trình này là cực chậm; vì thế chúng có mối tương quan bị giới hạn đối với các phản ứng của CO2 khí quyển trong việc thoát ra trong hàng trăm năm sau. Trong thời gian gần đây, nồng độ CO2 khí quyển vẫn tiếp tục theo đà suy giảm kể từ khoảng 60 triệu năm trước, và ở đây cũng có chứng cứ địa hóa học cho thấy nồng độ đã nhỏ hơn 300 µL/L vào khoảng 20 triệu năm trước. Nồng độ CO2 thấp có thể đã là tác nhân kích thích cho sự tiến hóa của các thực vật [[Sự cố định carbon C4|C4]], là những loài đã tăng đáng kể về số lượng trong khoảng 7–5 triệu năm trước. Mặc dù các nồng độ CO2 thời đó đã vượt quá trong vòng các kỷ nguyên địa chất diễn ra sớm hơn, các nồng độ carbon dioxide hiện nay có lẽ là cao hơn so với bất kỳ thời gian nào trong vòng 20 triệu năm qua [5][liên kết hỏng] nhưng lại là thấp hơn so với bất kỳ thời gian nào trong lịch sử nếu ta nhìn vào thang thời gian dài hơn 50 triệu năm.
Thủy quyển Trái Đất[sửa|sửa mã nguồn]
Các đại dương của Trái Đất chứa một lượng khổng lồ carbon dioxide trong dạng những ion bicacbonat và cacbonat — nhiều hơn rất nhiều so với lượng CO2 trong khí quyển. Bicacbonat được tạo ra trong những phản ứng của đá, nước và carbon dioxide. Dưới đây là ví dụ về sự hòa tan calci cacbonat :CaCO3 + CO2 + H2O ⇌ Ca2 + + 2 HCO3 −Các phản ứng tương tự như như thế có xu thế tạo ra những biến hóa đệm của CO2 khí quyển. Các phản ứng giữa carbon dioxide và những loại đá không cacbonat cũng bổ trợ thêm bicacbonat vào biển cả, chúng sau đó phản ứng theo chiều ngược lại của phản ứng trên để tạo ra những loại đá cacbonat và giải phóng 50% những bicacbonat thành CO2. Hàng trăm triệu năm qua chúng đã tạo ra một lượng lớn đá cacbonat. Nếu toàn bộ những loại đá cacbonat trong lớp vỏ Trái Đất được chuyển hóa ngược lại thành carbon dioxide thì lượng khí này sẽ nặng gấp 40 lần hàng loạt khí quyển .Phần đa phần của CO2 được bổ trợ vào khí quyển sau cuối sẽ bị những đại dương hấp thụ trong dạng những ion bicacbonat, nhưng quy trình này phải mất hàng trăm năm do phần đông nước biển lại không ở gần mặt phẳng .
Trong ngoài hành tinh[sửa|sửa mã nguồn]
Carbon dioxide là thành phần chính của khí quyển Sao Hỏa, và là một thành phần quan trọng của khí quyển Sao Kim. Có giả thuyết cho rằng vào thời kỳ hệ Mặt Trời mới hình thành, những hành tinh nằm ở vòng trong ( Trái Đất, Sao Hỏa, Sao Kim ) đều có khí quyển khá giống nhau và chứa nhiều thán khí. Thán khí cũng xuất hiện ở dạng băng khô trên những sao chổi .Chất khí này đã được quan sát là xuất hiện ở khoảng chừng không ngoài hành tinh, gần những sao thuộc thế hệ 2 hoặc thế hệ 3, nơi mà mẫu sản phẩm của quy trình phản ứng nhiệt hạch trong những sao đã tích tụ nhiều carbon và oxy. Có thể đặt giả thuyết rằng chất khí này xuất hiện trong khí quyển của những hành tinh thuộc vòng trong bay quanh những sao thuộc thế hệ từ 2 trở đi .
Carbon dioxide là một trong các khí đầu tiên được miêu tả như là chất hiện hữu trong không khí. Vào thế kỷ XVII, nhà hóa học người Flanders là Jan Baptist van Helmont đã quan sát thấy khi ông đốt than củi trong bình kín thì khối lượng còn lại của tro là thấp hơn so với khối lượng nguyên thủy của than củi. Diễn giải của ông là phần còn lại của than củi đã được biến tố thành chất không nhìn thấy mà ông gọi là “khí” hay “linh hồn hoang dã” (spiritus sylvestre).
Các thuộc tính của carbon dioxide được nhà vật lý người Scot là Joseph Black điều tra và nghiên cứu nhiều hơn trong thập niên 1750. Ông phát hiện ra là đá vôi ( calci cacbonat ) hoàn toàn có thể nung nóng hay giải quyết và xử lý bằng những axit để sinh ra khí mà ông gọi là ” không khí cố định và thắt chặt “. Ông quan sát thấy không khí cố định và thắt chặt nặng hơn không khí và không tương hỗ sự cháy cũng như sự sống của động vật hoang dã. Ông cũng phát hiện là nó hoàn toàn có thể, khi cho chạy qua dung dịch nước của vôi tôi ( calci hydroxide ) làm kết tủa calci cacbonat và sử dụng hiện tượng kỳ lạ này để minh họa rằng carbon dioxide là loại sản phẩm của sự hô hấp của động vật hoang dã và lên men vi sinh vật. Năm 1772, Joseph Priestley sử dụng carbon dioxide tạo ra từ phản ứng của axit sunfuric với đá vôi để điều chế nước soda, ví dụ tiên phong được biết của đồ uống cacbonat hóa nhân tạo .
Carbon dioxide được Humphrey Davy và Michael Faraday hóa lỏng lần đầu tiên năm 1823 bằng tăng áp suất. Mô tả đầu tiên về carbon dioxide rắn là của Charles Thilorier, là người năm 1834 đã mở thùng chứa carbon dioxide lỏng bị nén, chỉ để tìm sản phẩm được tạo ra do bị làm lạnh vì sự bay hơi nhanh của carbon dioxide lỏng và thấy “tuyết” của CO2 rắn.
- Friederike Wagner, Bent Aaby và Henk Visscher (2002) Rapid atmospheric CO2 changes associated with the 8,200-years-B.P. cooling event, PNAS 99 (19): 12011-12014 DOI: 10.1073/pnas.182420699
- Andreas Indermühle, Bernhard Stauffer, Thomas F. Stocker (1999) Early Holocene Atmospheric CO2 Concentrations, Science 286 (5446): 1815 DOI: 10.1126/science.286.5446.1815a Early Holocene Atmospheric CO2 Concentrations Science URL truy cập 26 tháng 5 năm 2005
- H.J. Smith, M Wahlen và D. Mastroianni (1997) The CO2 concentration of air trapped in GISP2 ice from the Last Glacial Maximum-Holocene transition, Geophysical Research Letters 24(1) 1-4
- Joseph Priestley (1772) Observations on Different Kinds of Air, Philosophical Transactions 62: 147-264
- Humphry Davy (1823) On the Applicatin of Liquids Formed by the Condensation of Gases as Mechanical Agents, Philosophical Transactions 113: 199-205
Liên kết ngoài[sửa|sửa mã nguồn]
Source: https://blogchiase247.net
Category: Hỏi Đáp






